Par Pascale Santi Publié le 11 février 2019
Les soins pour lutter contre cette maladie touchant 120 000 personnes en France ne permettent généralement que de retarder et d’alléger les symptômes.
Des thérapies cellulaires pourraient-elles freiner la progression de certaines formes de sclérose en plaques (SEP), voire les faire régresser ? Connue principalement dans le domaine de l’oncologie depuis près de cinquante ans, l’autogreffe de cellules souches hématopoïétiques (CSH), issues de la moelle osseuse, qui consiste à « nettoyer » le système immunitaire, peut être une approche thérapeutique dans certaines maladies auto-immunes, et notamment la SEP. Une nouvelle étude publiée dans Journal of the American Medical Association (JAMA), le 15 janvier, confirme les résultats encourageants obtenus depuis vingt ans en Europe.
Fin 2018, environ 3 000 autogreffes de CSH avaient été réalisées pour des maladies auto-immunes en Europe, dont quelque 1 280 chez des patients touchés par la SEP, selon les données du registre de la Société européenne de greffe de moelle (European Society for Blood and Marrow Transplantation, EBMT). Mais seuls dix-huit patients atteints de SEP ont été traités en France. Comment expliquer ce retard ?
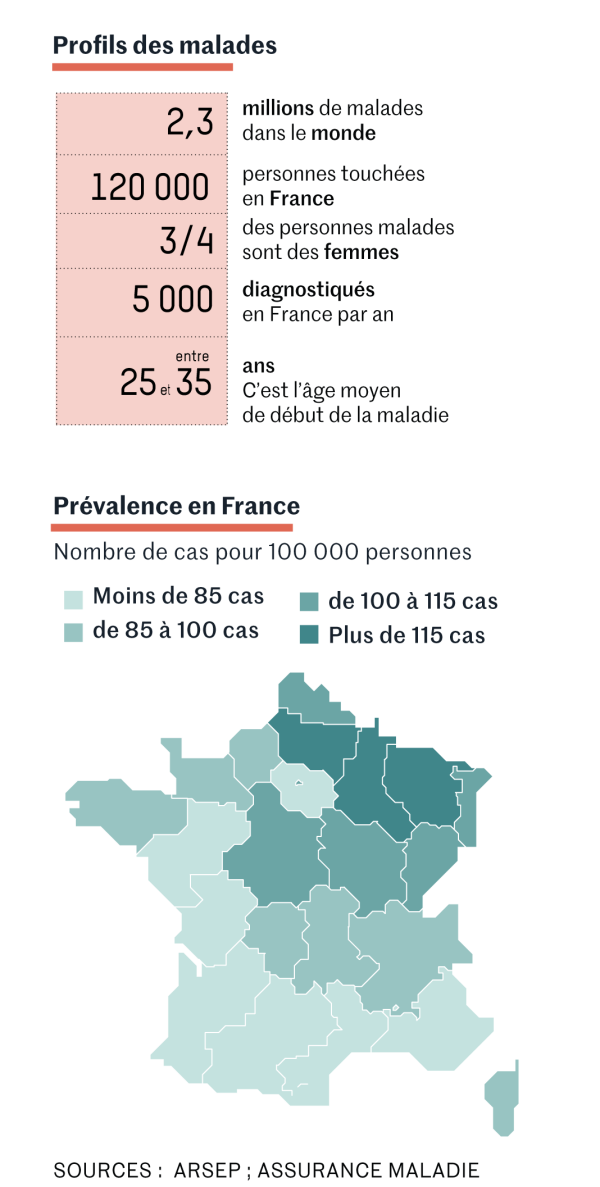
Rappelons d’abord ce qu’est la sclérose en plaques. Maladie à la fois inflammatoire et neurodégénérative, elle est extrêmement hétérogène. Touchant près de 120 000 personnes en France, pour les trois quarts des femmes, elle se déclare de plus en plus jeune, selon les derniers chiffres de la Fondation Aide à la recherche sur la sclérose en plaques (Arsep). Dans cette maladie auto-immune, les cellules immunitaires, en particulier les lymphocytes, en viennent à s’attaquer à la gaine de myéline qui protège et isole les fibres nerveuses du système nerveux central.
« Une affection polymorphe »
Cette dysfonction du système immunitaire provoque des « plaques inflammatoires » disséminées dans le cerveau et la moelle épinière, et peut entraîner des lésions qui provoquent des perturbations motrices, sensitives, visuelles et cognitives, telles que baisse de la vue, faiblesse musculaire, fourmillements dans les bras ou les jambes…
La majorité des personnes atteintes de SEP présentent des formes dites « rémittente-récurrente », qui se caractérisent par des poussées aiguës, suivies de rémission, avec ou sans séquelles. Après des années, la forme secondaire progressive de la maladie survient et engendre des lésions et un handicap. La maladie peut être aussi totalement bénigne, avec une ou deux poussées et aucune séquelle. En 1868, Jean-Martin Charcot, l’un des premiers neurologues à décrire la maladie, à l’hôpital de la Salpêtrière, évoquait déjà « une affection polymorphe par excellence ».
« Depuis une quinzaine d’années, la photographie de la maladie a complètement changé, avec une panoplie thérapeutique solide », explique le neurologue Jean Pelletier (CHU La Timone, Marseille), président du conseil médico-scientifique de la Fondation Arsep. Les immunomodulateurs (interférons-bêta et copolymères) sont disponibles depuis une vingtaine d’années, complétés plus récemment par des traitements immunosuppresseurs par voie orale (diméthyl fumarate, tériflunomide).
D’autres traitements dits de deuxième ligne (mitoxantrone, natazimulab, fingolimod, ocrelizumab, alemtuzumab, Cladribine) sont utilisés soit parce que la maladie est d’emblée agressive, soit parce que les premiers ne fonctionnent pas. Ce sont des anticorps monoclonaux ou des immunosuppresseurs. Ces médicaments, parfois inefficaces, ne sont pas sans effets secondaires, parfois graves, principalement des infections (favorisées par l’immunodépression) et des maladies auto-immunes.
Des défenses immunitaires « remises à zéro »
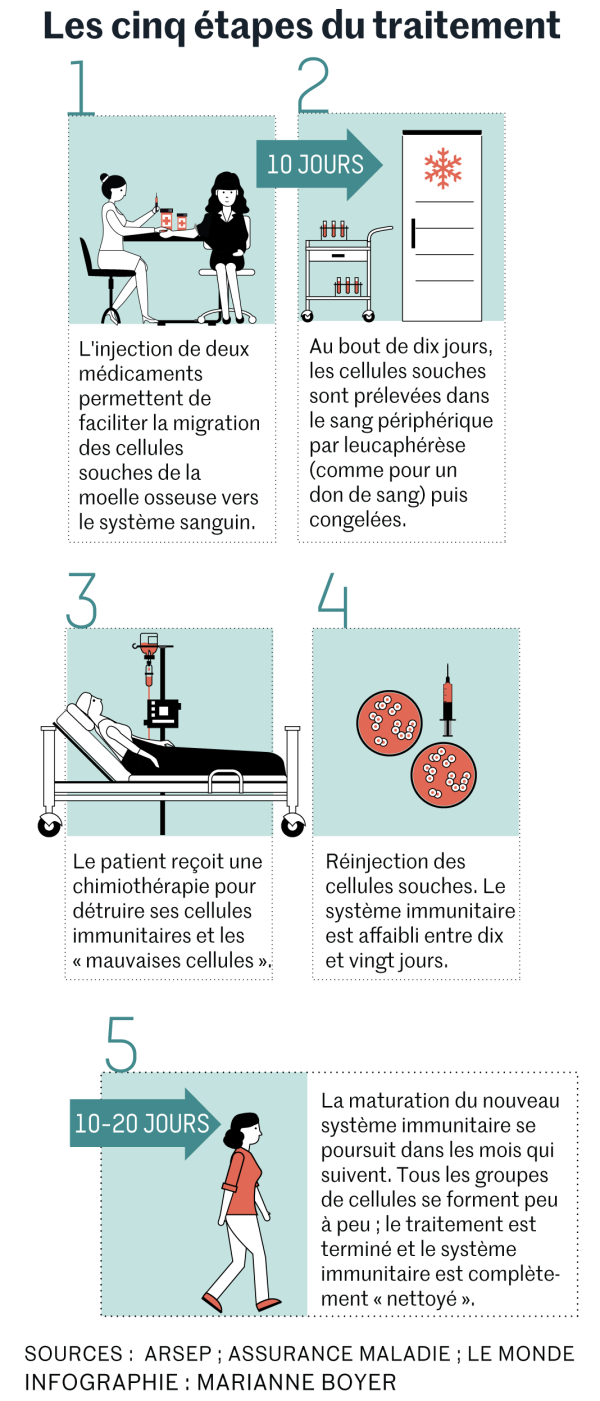
Moins connue, l’autogreffe de CSH consiste à « réinitialiser » le système immunitaire défaillant. Les cellules souches hématopoïétiques sont prélevées dans le sang du patient. Celui-ci reçoit ensuite une chimiothérapie intensive qui détruit son système immunitaire – on parle d’aplasie. Les cellules T autoréactives, qui possèdent la mémoire de la maladie, sont ainsi éliminées. Congelées pendant la phase de chimiothérapie, les cellules souches hématopoïétiques sont réinjectées au patient, qui reconstitue alors ses défenses immunitaires « remises à zéro ».
Les chercheurs y travaillent depuis une vingtaine d’années, à l’instar de l’hématologue Richard Burt (Feinberg School of Medicine de Northwestern University de Chicago).
L’étude qu’il vient de publier dans JAMA porte sur 110 patients atteints de SEP dans la forme « rémittente-récurrente », dont 73 femmes, réfractaires à trois médicaments, et qui avaient vu leurs symptômes s’aggraver au moins deux fois dans l’année. Agés en moyenne de 36 ans, la moitié des patients a reçu un traitement standard et l’autre a subi une greffe de cellules souches.
Résultat : un an plus tard, les patients qui ont bénéficié du traitement d’autogreffe de CSH présentaient une progression moins rapide, seuls trois d’entre eux (5 %) ont vu la maladie évoluer, contre 60 % de ceux qui avaient un traitement médicamenteux. De même, leur score de handicap neurologique EDSS et la qualité de vie se sont améliorés pour le premier groupe. Passer d’un score d’EDSS de 4 à 3 peut vouloir dire qu’il n’y a plus de problème de marche. Les IRM ont également révélé une régression des lésions cérébrales. Par ailleurs, aucun décès ni complication grave ne sont survenus.
Des patients sélectionnés
D’autres études avaient déjà montré que l’autogreffe de CSH pouvait supprimer les traces de la maladie pendant quatre à cinq ans chez 70 % à 80 % des patients, un taux supérieur à celui obtenu avec n’importe quel autre traitement, soulignait une étude publiée dans Nature en juillet 2017. De même, une équipe canadienne menée par Harold Atkins et Mark Freedman (université d’Ottawa) a publié dans The Lanceten 2016 une étude montrant que le traitement par greffe a pratiquement arrêté toute nouvelle poussée chez vingt-quatre patients âgés de 18 à 50 ans atteints des formes progressives, évoluées, et de mauvais pronostic. En revanche, une personne était décédée.
« L’article du Lancet a remis les projecteurs sur cette technique. C’est un traitement intéressant, mais il doit être optimisé. Par exemple, des questions demeurent sur les cellules souches qui doivent être sélectionnées et sur la chimiothérapie qui doit être proposée », souligne Caroline Papeix, neurologue à la Pitié-Salpêtrière. Les auteurs eux-mêmes plaidaient pour une confirmation de leurs travaux par d’autres essais randomisés, notamment en comparant l’autogreffe aux médicaments les plus puissants du marché.
Pour l’interniste Dominique Farge, spécialiste des maladies auto-immunes à l’hôpital Saint-Louis, à Paris, qui travaille sur cette question depuis une vingtaine d’années, « l’autogreffe peut être une alternative aux traitements de deuxième ligne, à condition de bien sélectionner les patients ».
Lire aussi
La thérapie cellulaire pour les maladies auto-immunes
C’est tout l’enjeu. Ce traitement n’est pas pour tous les patients, loin de là. Il peut être efficace dans des cas bien particuliers pour des formes qui évoluent par poussées ou progressivement, de façon rapide et agressive, dites « rémittentes-récurrentes », avec un délai d’évolution court, sans handicap sévère et ayant toujours une activité inflammatoire, visible notamment à l’IRM. C’est le sens des recommandations précises qui ont été édictées par la Société francophone de greffe de moelle et de thérapie cellulaire (SFGM-TC), en lien avec la Société francophone de sclérose en plaques (SFSEP), et publiées dans le Bulletin du cancer fin 2017.
Pas sans risques
Dans les faits, chaque cas doit être discuté, dans le cadre de réunions de concertation pluridisciplinaires. « Nous venons de passer quatre heures aujourd’hui avec mon équipe et le neurologue pour examiner une greffe, car le patient doit être appréhendé dans sa globalité. On doit scruter les fonctions cardiaques, respiratoires, rénales pour prévenir d’éventuelles complications lors de la phase d’aplasie », insiste la professeure Farge.
« Le message fort est de dire que cette approche thérapeutique a vraisemblablement toute sa place dans la prise en charge de cette maladie, en respectant un certain nombre de critères liés à la forme de la maladie, son ancienneté, et surtout l’existence d’une activité inflammatoire », souligne Jean Pelletier. La discussion concernant les indications doit selon lui être partagée dans les centres experts SEP (CRC SEP, centre de ressources et de compétences SEP), ainsi qu’avec les différents spécialistes impliqués.
Praticiens et patients peuvent aussi contacter les membres du réseau Mathec (Maladies auto-immunes et thérapie cellulaire), développé au niveau national par l’équipe et situé dans l’hôpital Saint-Louis, en lien avec les experts de la SFGM-TC et de la SFSEP.
Efficace, cette approche n’est toutefois pas sans risque… La mortalité se situait autour de 5 % lors des premiers essais, un chiffre jugé éthiquement inacceptable. Mais, pour le docteur Paolo Muraro, neurologue à l’Imperial College de Londres, qui a lui même réalisé de nombreux travaux sur l’autogreffe, le taux de mortalité global associé à l’autogreffe pour la SEP est aujourd’hui inférieur à 1 %, a-t-il indiqué dans un article de Science le 15 janvier. Les effets sont principalement des infections (favorisées par l’immunodépression) en raison de la faiblesse du système immunitaire, une grande fatigue…
« Il faut tenir compte de la balance bénéfices/risques entre une thérapeutique efficace, mais avec un risque de mortalité et de morbidité non négligeable, bien supérieur aux risques des autres traitements », explique Jean Pelletier.
Ce traitement ne fait pas encore partie des recommandations de la Haute Autorité de santé (HAS), qui sont assez anciennes sur la SEP. La HAS indique ne pas avoir été saisie de cette approche. Certains neurologues se réfugient derrière ce silence pour expliquer leur frilosité. Pourtant, les recommandations de la SFGM-TC sont claires.
Une affaire de neurologues
« Notre souhait est de démocratiser ces pratiques et de permettre l’accès aux patients, mais pas de considérer que la greffe de moelle est pour tout le monde », précise la professeure Dominique Farge. Il s’agit aussi d’éviter que des malades ne se rendent à l’étranger dans des cliniques privées pas toujours recommandables, alors que les indications ne sont pas valides.
Le faible écho rencontré par cette approche est d’autant plus surprenant que, en France, elle a été étudiée depuis vingt ans, grâce à quelques médecins, dont la professeure Farge. Elle a à maintes reprises rencontré la communauté des neurologues, qui préfèrent généralement continuer dans la voie des biothérapies. « Mes lettres sont restées vaines », regrette l’interniste. Les débats ont pu être vifs il y a quelques années, certains experts critiquant la greffe jugée à l’époque trop dangereuse.
Le neurologue Patrick Vermersch (CHRU de Lille) a lui aussi été l’un des premiers à en parler à ses équipes. « C’est une thématique qui nous intéresse depuis une vingtaine d’années », confirme Louis Terriou, son binôme en immunologie au CHRU de Lille. Le premier patient greffé il y a treize ans, âgé de moins de 30 ans, mène aujourd’hui une vie presque normale…
Le neurologue Olivier Gout, de la Fondation Rothschild, reste plutôt réservé : « Très peu de neurologues y sont favorables, en raison du risque, de décès bien sûr, mais aussi d’infection, surtout dans les six mois après la greffe. » Certes, elle « semble avoir une certaine efficacité, mais est-elle plus efficace qu’un autre traitement tel un anticorps monoclonal, de type alemtuzumab (Campath) ? Cela n’a pas été évalué », poursuit le docteur Gout.
Même réserve pour Caroline Papeix : « Cela doit rester exceptionnel. Il faut prouver qu’il n’existe pas d’alternative thérapeutique, le patient doit être informé des risques encourus, d’autant plus que cela ne fait pas partie des recommandations validées. Il faut rester prudent et ne pas donner de faux espoirs. » Selon elle, la décision revient aux neurologues.
Enjeux économiques
La greffe, un traitement de niche ? Pour le pionnier Richard Burt, cité par Science, environ 15 % à 20 % des personnes atteintes de SEP seraient éligibles à cette approche. Un chiffre qui semble exagéré pour les spécialistes français. « Le nombre de patients est sans doute plus faible, peut-être un ou deux malades par an et par CHU. Mais il faudrait au minimum que tous les cas soient discutés pour évaluer un tel traitement », d’après le docteur Terriou.
« Malheureusement, on voit des patients arriver trop tard, avec des troubles cognitifs, en fauteuil roulant… alors que l’autogreffe de CSH aurait dû être envisagée plus précocement », regrette-t-il. « Nous avons certains patients pour lesquels il faut taper fort et vite, contrairement à la stratégie très conservatrice de beaucoup de neurologues », confirme Patrick Vermersch, pour qui « les progrès dans la procédure et une meilleure sélection des patients rendent aujourd’hui ce traitement moins risqué ».
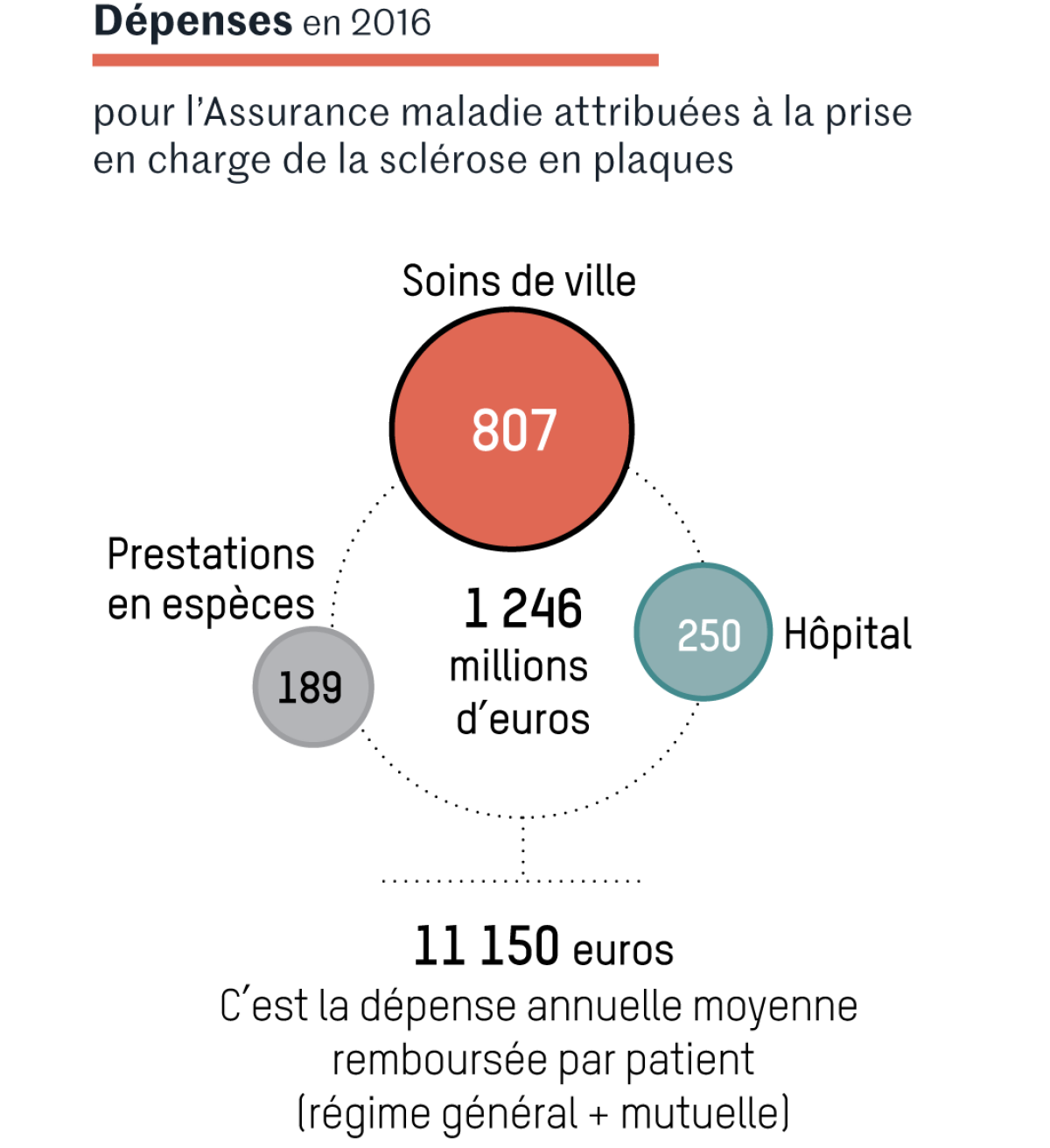
Au-delà des risques, certains expliquent les réserves vis-à-vis de la greffe par des raisons économiques. La plupart des traitements pour traiter la SEP sont très onéreux, autour de dizaines de milliers d’euros par an, tandis qu’une greffe (moins de 50 000 euros en moyenne) peut permettre de s’en passer. « Ce traitement de l’autogreffe est emblématique des enjeux économiques dans la santé et de l’importance de l’industrie pharmaceutique dans le financement des études. Elle n’a aucun intérêt à encourager une telle étude comparant l’autogreffe et des médicaments, surtout si l’on montre qu’elle est aussi efficace que les traitements immunomodulateurs », explique le neurologue Jean-François Chermann. Point positif, pour Dominique Farge : « Cette année, enfin, les neurologues commencent à bouger. »



Aucun commentaire:
Enregistrer un commentaire