Propagation, mortalité, impact du confinement... Si « tous les modèles sont faux, certains sont utiles », disent les statisticiens, qui disposent d’outils pour anticiper la suite de la pandémie.
Combien de morts du Covid-19 ? Combien d’hospitalisés en réanimation ? Combien de temps le confinement durera-t-il ? Autant de questions brûlantes auxquelles s’attaque la science de la modélisation… avec difficulté.
Le 12 mars, face aux prédictions d’une submersion du système hospitalier avancées par une équipe anglaise de l’Imperial College (Londres), la France s’est engagée dans une stratégie de confinement poussé. « Les modèles sont un signal parmi d’autres. La situation italienne, mais aussi toutes les connaissances accumulées sur des épidémies précédentes allaient dans le sens de cette décision pour soulager le système de santé », relativise Simon Cauchemez, chercheur à l’Institut Pasteur, spécialiste en modélisation et membre du conseil scientifique Covid-19 mis en place par le gouvernement.
Il n’y avait en effet pas besoin du modèle anglais pour être inquiet. Un « vieux » modèle des années 1930 et les premières données chinoises sur le nouveau coronavirus fournissent assez vite aux spécialistes des estimations d’au moins 50 % de personnes infectées au pic de l’épidémie, et donc plus de 300 000 morts en France avec une hypothèse de seulement 1 % de létalité due au virus.
Deux approches
Les scientifiques disposent en fait de deux grandes manières pour appréhender la dynamique d’une épidémie, soit par des approches dites compartimentales, soit par des méthodes multi-agents ou « individus centrés ». La première remonte aux années 1930 et la seconde au début des années 2000.
En 1927, 1932 et 1933, deux Ecossais, Anderson Gray McKendrick et William Ogilvy Kermack, – le premier a dirigé un Institut Pasteur en Inde –, publient trois études dans les comptes rendus de la Royal Society (l’équivalent de l’Académie des sciences en France). Ces articles sont si marquants qu’ils furent republiés en 1991 dans Bulletin of Mathematical Biology. Le modèle qu’ils y développaient décrivait très bien un épisode de peste en Inde en 1906.
L’idée est de mettre les individus en trois compartiments : les « sains », S, susceptibles d’être contaminés, les « infectés », I, et les « retirés », R, ceux qui ne sont plus malades, car soit morts, soit immunisés après une infection. Des taux de passage décrivent les flux entre ces trois catégories, comme le taux de contamination (passage de S à I) et le taux de guérison (ou durée de l’infection, passage de I à S), ce qui fournit des équations faciles à résoudre. Plus tard, ces modèles seront baptisés SIR. En conclusion de leur premier article, les deux mathématiciens notaient, message rassurant, qu’« une épidémie, en général, prend fin avant que la population sensible n’ait été éradiquée ». Autrement dit, les lois mathématiques protègent une partie de la population : tout le monde n’a pas besoin d’être touché pour observer un reflux.
Moteur infernal
La force de cette approche est qu’un seul paramètre, que les Ecossais n’avaient pas formellement baptisé, donne une intuition simple de la dynamique épidémique et de ce qui peut se passer. Il s’agit du taux de reproduction, c’est-à-dire le nombre de personnes qu’un infecté peut contaminer. S’il vaut 2, cela signifie qu’un malade contaminera deux personnes, qui ensuite, au total, en contamineront 2×2 = 4, puis 2×2×2 = 8…
Le moteur infernal est enclenché, et le nombre de cas suit une loi exponentielle, qui, selon les légendes, a ruiné bon nombre d’empereurs. Ces derniers, croyant attribuer une modique récompense, acceptaient des accords sibyllins consistant à doubler chaque jour le nombre de grains de riz sur les cases d’un échiquier. Même partant d’un seul grain, à la fin, le total d’environ des milliards de milliards de grains dépasse de loin la production mondiale.
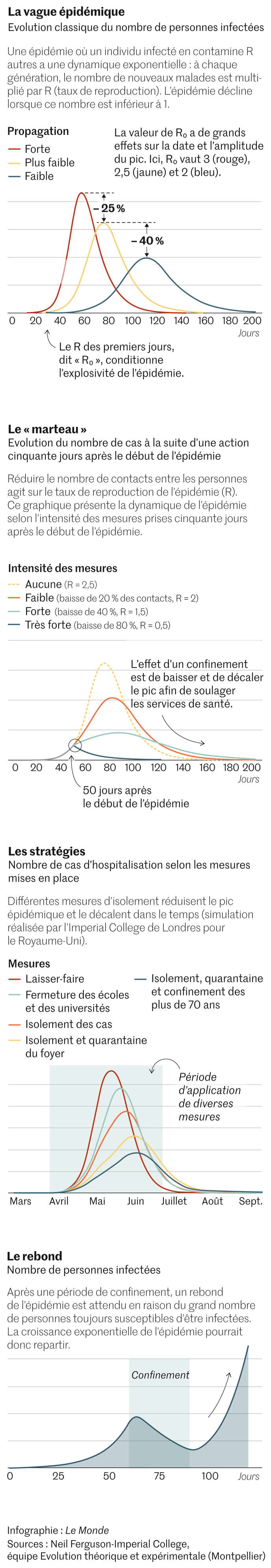
En épidémiologie, cette constante macabre, baptisée R0, au début de la flambée, est parmi la première que les statisticiens essaient d’évaluer. Sa valeur exacte joue beaucoup sur les prévisions. Passer de R0 = 3 à R0 = 2,5 décale le pic épidémique de trente jours et le fait baisser de presque 25 %. « Estimer R0 est simple en théorie. On compte le nombre de cas secondaires, et on divise par le nombre de cas primaires, rappelle Pierre-Yves Boëlle, de l’Institut Pierre-Louis d’épidémiologie et de santé publique. Mais c’est compliqué en pratique ! »
Comprendre l’intérêt du confinement
En effet, cette méthode suppose d’identifier les cas, de retracer leur historique et de repérer les contaminés secondaires. En pratique, on étudie la courbe épidémique, le nombre de cas ou de morts en fonction du temps, car sa croissance exponentielle, est reliée au R0. Mais tout dépend de la qualité des données : tous les cas sont-ils détectés ? Les morts attribuables à la maladie sont-ils tous comptés ?
Résultat, par exemple pour la France, selon Samuel Alizon, chercheur CNRS à Montpellier en évolution des maladies infectieuses, qui utilise des outils développés par le groupe de Pierre-Yves Boëlle pour calculer le R0, ce dernier varie dans le cas du Covid-19 entre 2,39 et 2,58.
Ce paramètre permet aussi de comprendre simplement l’intérêt d’un confinement. Il dépend en effet notamment du nombre de contacts entre les gens et de la probabilité de contamination. Réduire les contacts diminue le taux de reproduction, et donc la flambée. Au pic, le nombre de nouveaux cas chute car le taux de reproduction devient inférieur à 1 : une personne contamine moins d’une nouvelle personne.
Autre enseignement « utile », au moment du pic, le pourcentage de la population touchée est d’environ 1-1/R0, ce qui correspond aussi au pourcentage à atteindre pour immuniser le groupe. Si R0 vaut 2, c’est 50 %. Si R0 vaut 3, c’est 66 % environ. Il permet aussi d’estimer rapidement le pourcentage total de personnes infectées (un R0 de 2 donne environ 80 %).
« Le modèle SIR a beau être simpliste, dans beaucoup de cas, il marche. Surtout, il est souvent implicite dans nos raisonnements, à cause de l’importance du R0 », explique Samuel Alizon.
Simulateurs en ligne
Mais le vieux rafiot écossais a quand même été modifié. Il est ainsi possible d’ajouter des compartiments supplémentaires. On peut avoir une population « exposée » qui incube le virus avant d’être « infectée ». On peut ajouter, notamment dans le cas de l’épidémie due au SARS-CoV-2, des étiquettes « asymptomatiques » pour les gens qui contaminent avec plus ou moins de probabilité leurs congénères, probabilité qui reste encore un mystère pour le nouveau coronavirus. On peut aussi, notamment pour anticiper la surcharge hospitalière, créer des compartiments « malades sévères » ou « malades non sévères »…
Récemment, plusieurs équipes ont ainsi proposé leurs SIR améliorés. A l’université de Bâle, l’équipe de Richard Neher utilise sept compartiments, pour simuler l’évolution de la maladie. Il est même possible, au cours du temps, de changer le taux de reproduction, pour réduire la transmission et « voir » l’effet d’un équivalent d’une situation confinée.
La technique étant relativement simple à mettre en œuvre, beaucoup de simulateurs sont proposés en ligne, comme celui de l’équipe suisse ou comme ceux d’« amateurs », tel celui de Gabriel Goh, spécialiste d’apprentissage machine, qui, avec onze « curseurs », permet de se faire des idées de la propagation d’une maladie.
« Matrices de contact »
Malgré ces raffinements, cela ne suffit pas. Anderson McKendrick et William Kermack avaient prévenu : ces modèles ne marchent que pour une population homogène, où tout le monde infecte tout le monde de la même manière. Or les populations réelles sont hétérogènes, avec des densités différentes sur le territoire et, surtout, n’ont pas le même âge. Or un enfant n’a pas la même susceptibilité à une maladie qu’un adulte ou qu’une personne âgée. Il n’a pas non plus le même nombre de contacts quotidiens que ses parents ou grands-parents.
D’où l’idée d’améliorer la description en ajoutant des « compartiments » en classe d’âge, par tranche de cinq ans. Chacun des paramètres précédents aura donc une valeur différente pour chaque tranche. Fort heureusement, de scrupuleux statisticiens ont estimé ces données de contact pour plusieurs pays. En France, par exemple, un enfant de moins de 5 ans a trois fois plus d’interactions quotidiennes avec des enfants de son âge qu’avec des personnes de 30-34 ans. Les adolescents de 15-19 ans sont les plus « tactiles » (dans leur tranche d’âge), et les Français ont presque deux fois plus de contacts que les Allemands à l’intérieur de cette tranche.
« Ces matrices de contact changent la dynamique d’une épidémie », insiste Pascal Crépey, de l’Ecole des hautes études en santé publique à Rennes. Son modèle, en ligne le 20 mars, tient compte de cet effet et prédit l’engorgement hospitalier actuel en fonction de différents R0. Dans l’hypothèse où R0 = 3, toutes les régions d’ici au 15 avril seraient débordées. La moitié résisterait si R0 = 2,25. Et cela sous l’hypothèse, désormais fictive, qu’aucune mesure pour réduire les transmissions n’est prise.
Approche multi-agents
Sa consœur Vittoria Colizza, à l’Inserm, a aussi étudié l’effet des fermetures d’écoles sur la propagation. Car, même si une telle mesure n’avait jamais été prise, il existe des données de « contacts » en période scolaire et en période de vacances (proche d’une situation de fermeture). Le modèle à compartiments, mis en ligne le 14 mars, estimait ainsi une réduction de 10 % du pic épidémique en fermant les écoles. Mais le 16 mars, un confinement plus dur était annoncé, rendant caduques ces estimations…
Même philosophie, publiée dans The Lancet le 25 mars, par une équipe de la London School of Economics à propos de la ville chinoise de Wuhan, épicentre de l’épidémie. Ce modèle compartimenté prédit qu’une levée des mesures de confinement en avril baisserait de plus de 90 % les cas quotidiens par rapport à une levée en mars.
A force d’aller dans les détails, les chercheurs ont voulu pousser jusqu’au bout et zoomer jusqu’à l’individu lui-même. Pourquoi diviser la population en dix-sept tranches quand les ordinateurs peuvent facilement traiter les situations de chaque cas individuel, fussent-ils des millions ? Cette approche, dite multi-agent ou individu-centrée, a été développée depuis une quinzaine d’années et constitue la seconde grande famille de modèles.
Comme pour les modèles SIR, les principes sont assez simples. A chaque individu du modèle sont attachés un âge, un lieu d’habitation, des enfants, un lieu de travail… Il peut bouger dans l’espace, contraint par les données connues de mobilité, de densité… Arrive une maladie avec ses propriétés propres de temps d’incubation, d’infection, de contagiosité. Ces deux types d’informations sont mélangés, et la simulation est lancée. Elle est forcément aléatoire (on met une personne infectée au hasard, les gens bougent de façon erratique…), et elle est reproduite plusieurs centaines de fois, afin d’en tirer des enseignements moyens sur le nombre de nouveaux cas, d’hospitalisations…
Mêmes résultats
A l’Imperial College, l’équipe de Neil Ferguson est experte en la matière depuis sa simulation présentée en 2005 dans Nature, de la grippe H5N1 en Asie du Sud-Est par ces méthodes. Ces chercheurs l’ont également appliquée au Covid-19 pour mesurer l’effet de différentes restrictions de circulation et inspirer les gouvernements.
D’autres l’ont fait à l’échelle de Singapour dans le même but. Comme ils l’expliquaient dans The Lancet le 23 mars, la stratégie la plus efficace, pour réduire de 99 % le nombre d’infections est la panoplie complète : fermeture des écoles, quarantaine des malades et éloignement du travail. Mais là encore, tout dépend de plusieurs hypothèses, notamment celles sur le R0.
« Ces simulations sont plus réalistes, mais elles contiennent plus de paramètres et sont difficiles à interpréter, constate Simon Cauchemez, qui a travaillé avec Neil Ferguson et jongle avec les deux approches. Les approches multi-agents n’ont pas été utilisées en France car elles n’étaient pas nécessaires pour répondre aux questions posées. » Neil Ferguson lui-même, dans le dernier rapport de son équipe du 26 mars, reconnaît que le modèle SIR, qu’il a aussi utilisé, donne les mêmes résultats que ses simulations multi-agents, plus complexes.
En fait, à chaque problème, son modèle. « La règle est qu’on cherche le modèle le plus simple pour répondre à la question posée », résume Laura Temime, du Conservatoire national des arts et métiers.
Mais il faut faire vite, car les questions changent avec l’évolution de l’épidémie. Au début, lorsque le virus n’était qu’en Chine, il s’agissait de savoir quelle était la probabilité qu’il débarque en Europe. La réponse est venue de Vittoria Colizza qui a travaillé sans SIR ou multi-agents, « juste » en analysant les flux aériens entre pays et à l’intérieur de la Chine.
Barre d’erreurs
Puis les statisticiens se sont abîmé les yeux sur les cas chinois pour estimer le fameux R0, tandis que leurs collègues sur le terrain traquaient les patients atteints pour remonter la chaîne de contamination et identifier deux autres paramètres-clés, le taux de mortalité et le temps de génération (grosso modo le temps entre l’apparition des symptômes chez le premier et le second contaminé).
Ensuite, les modèles à compartiments chauffent pour anticiper la dynamique et les saturations des services de santé. Et très vite, les mêmes ou les versions multi-agent tournent pour estimer l’effet de diverses mesures (isolement des cas, quarantaines, fermeture d’écoles, arrêt de travail, confinement strict…). Laura Temime s’est lancée sur des microsimulations à l’échelle d’un hôpital pour savoir à qui donner les masques en priorité en cas de pénurie.
« Et maintenant, on veut savoir quoi faire après le confinement en étudiant diverses options, note Simon Cauchemez qui pense que le conseil scientifique devrait faire des recommandations cette semaine. Mais ce confinement est une situation inédite, et nous manquons forcément de données pour alimenter les modèles. » Les opérateurs téléphoniques pourraient être un recours. Orange a annoncé le 27 mars avoir passé un accord avec l’Inserm et l’équipe de Vittoria Colizza pour utiliser les données téléphoniques afin d’évaluer la mobilité en temps normal et en temps confiné.
« Le problème, ce n’est pas les modèles, mais leurs hypothèses et les données qui les nourrissent », indique Pascal Crépey en écho au célèbre adage des statisticiens, « Tous les modèles sont faux, mais quelques-uns sont utiles ». Le Covid-19 n’échappe pas à la règle. Quel est le taux de mortalité ? Quelle est la part des asymptomatiques contagieux et avec quelle efficacité transmettent-ils le virus ? Le virus pourrait-il muter ?
Pour ces raisons, chaque simulation est assortie non seulement de la traditionnelle barre d’erreurs mais aussi d’une analyse de sensibilité des résultats aux fluctuations des divers paramètres utilisés. Quelques dixièmes d’incertitude peuvent changer de plusieurs milliers un nombre de cas. « Les simulations sont à manier avec précaution en termes de communication », résume Pierre-Yves Boëlle. En outre, les prédictions initiales, où « on ne fait rien », sont souvent démenties avec le temps, car les gens changent leurs pratiques devant le risque.
Cependant les spécialistes se risquent à une prévision. La fin d’un confinement causera un rebond de la courbe épidémique car il n’y aura pas eu assez de « contaminés », donc « d’immunisés ». Comme le bon vieux modèle de 1927 le laisse entendre…

Aucun commentaire:
Enregistrer un commentaire